临床实验|媒体披露国产疫苗最新消息:进度全球领先,具备大规模量产能力
小新说
在接连经受武汉、北京两轮新冠肺炎疫情的“侵袭”之后 , 中国本土的新冠肺炎疫情基本上得到有效控制 。 然而 , 国门之外不断刷新人类历史记录的全球新冠肺炎大疫情时刻提醒着我们 , 新冠肺炎病毒所制造的威胁并未真正消除 。
后疫情时代 , 如何才能摘下口罩回归正常生活成为笼罩在公众心头的疑雾 。 包括美国顶级传染病专家安东尼·福奇在内的许多学者提出 , 疫苗不问世 , 我们已经无法彻底阻断疫情 。 而根据现有对于新冠肺炎病毒的认识 , 国内许多专家学者也认为 , 如果说这场疫情“阻击战”的上半场主要靠防治 , 那么下半场则主要依赖于疫苗的问世 。
所幸 , 最先走出新冠肺炎疫情风暴的中国在新冠病毒疫苗研发工作中目前也处于全球第一梯队的位置 。
近日 , 主要承担中国新冠病毒灭活疫苗研发任务的国药集团中国生物技术股份有限公司董事长杨晓明在接受环球时报专访时表示 , 乐观估计 , 国产新冠病毒灭活疫苗最快或于今年底或明年初上市 。 一起来了解——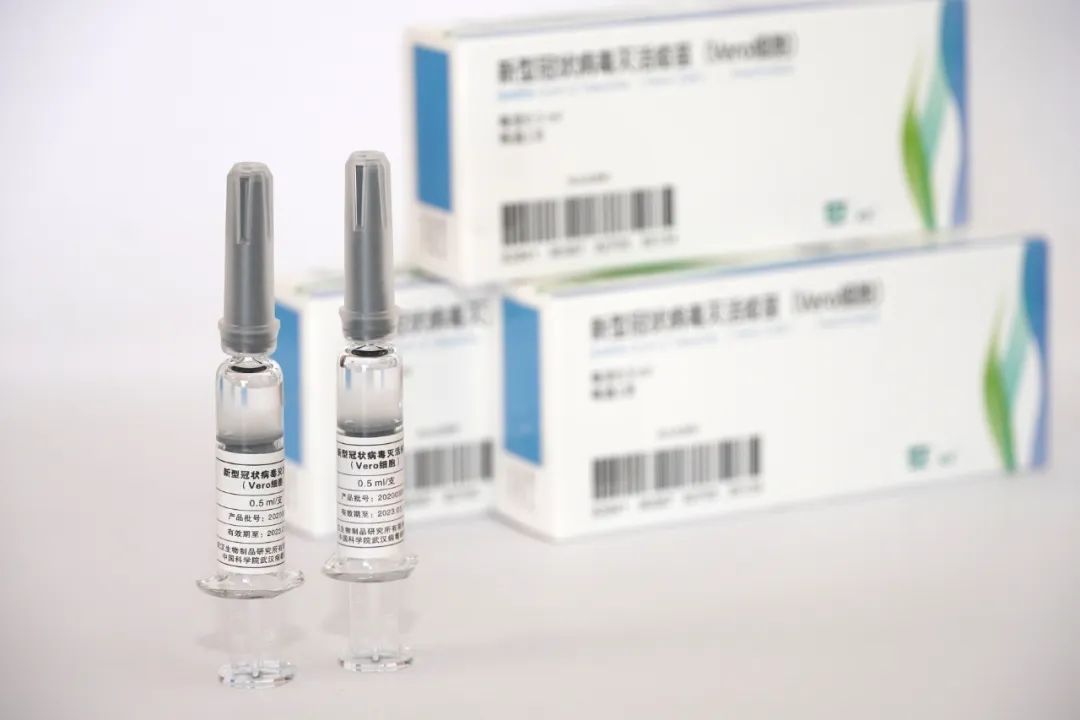
本文图片
新冠疫苗已成决战决胜疫情的“杀手锏”
据美国约翰斯·霍普金斯大学数据统计 , 截止2020年7月16日 , 全球共有一千三百五十余万人确诊感染新冠肺炎 , 死亡人数达到58万余人 , 其中美国的新冠确诊人数超过349万 , 死亡超过13万人 。 世卫组织7月12日发布的每日疫情报告显示 , 全球新冠肺炎确诊病例24小时内新增了230370例 , 创下了单日新高 。
不断刷新历史纪录的全球新冠疫情 , 预示着人类已经无法期待疫情自然消退 , 类似2003年非典疫情那样突然消失的情况很有可能不再上演 。 而全球新冠疫情的持续恶化也意味着西方某些国家提出的“群体免疫“构想彻底破产 , 疫苗成为终结新冠肺炎疫情的“最终武器”已经成为全球各国的共识 。 对于疫苗在新冠肺炎疫情“阻击战”中的特殊使命 , 科技部“863计划”疫苗项目首席科学家、中国生物技术股份有限公司董事长杨晓明表示 , 中国新冠疫情的有效控制 , 得益于中国政府采取了严格的隔离措施进行阻断 , 但是疫苗才是最终终结疫情最有力的武器 , 也是全国甚至全球恢复正常运转的关键所在 。 只有把安全、有效、足量的疫苗成功研发出来 , 尽快高效供应和使用 , 才是人类最终战胜新冠病毒的根本之策 。
“从人类发展历史来看 , 正是疫苗的出现和广泛使用 , 才真正终结了天花 , 消除了脊髓灰质炎 , 控制了麻疹、白喉、百日咳、破伤风等疾病 。 疫苗为人类降低传染病危害做出了巨大贡献 。 我们认为 , 新冠病毒疫苗正是决战决胜疫情的‘杀手锏’ 。 ”杨晓明称 。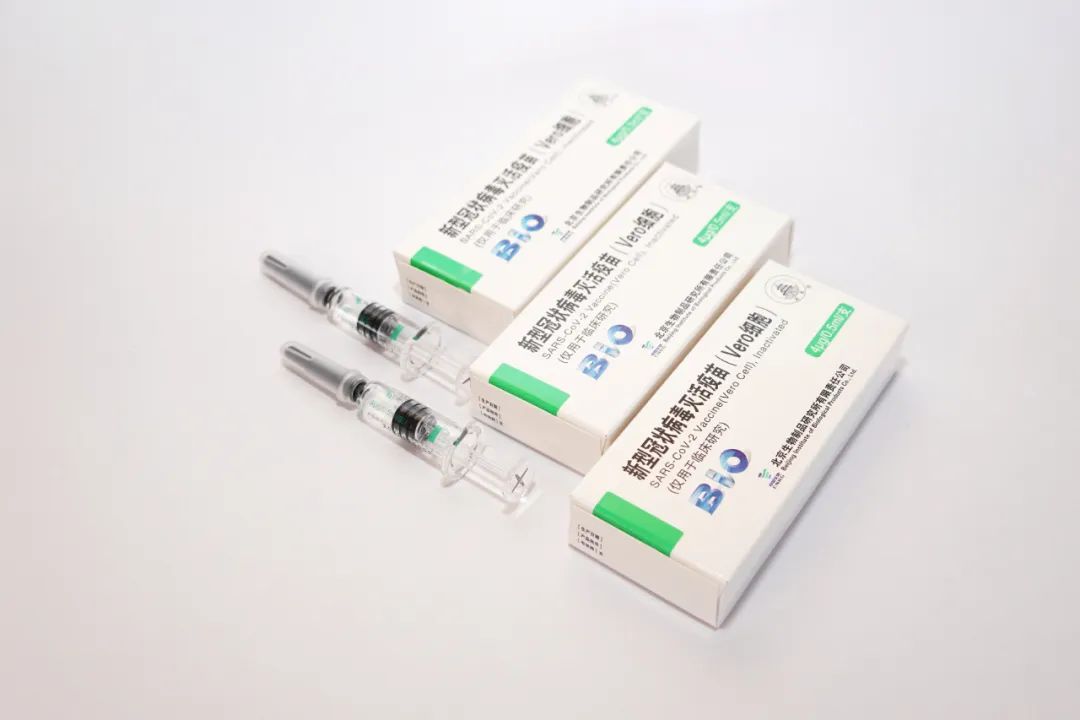
本文图片
试验、量产同步进行 , 力争满足全球接种需求
根据世卫组织公布的数据 , 目前全球已有超过100个新冠病毒疫苗项目同时在研 。 其中 , 中美英三个国家的疫苗项目均已进入了临床试验阶段 。 在2020年上半年 , 中国就有包括国药集团中国生物杨晓明挂帅的科研攻关领导小组、军事科学院军事医学研究院陈薇院士团队在内的至少6个团队的新冠疫苗进入临床试验阶段 , 成为全球研发新冠病毒疫苗成效最为显著的国家;美国则有三家 , 分别是莫德纳公司的mRNA疫苗、辉瑞公司的mRNA疫苗、INOVIO公司的DNA载体疫苗;此外 , 英国牛津大学研发的腺病毒载体疫苗也已进入临床试验阶段 。
而在迈入临床试验阶段的六款中国疫苗中 , 国药集团中国生物承担研发的灭活疫苗目前已经进入临床三期试验阶段 , 并已具备大规模量产的能力 , 各项进度均处于全球领先地位 。
据杨晓明介绍 , 2月1日 , 在新冠肺炎疫情肆虐之际 , 中国生物作为牵头单位获得了科技部国家重点研发计划“公共安全风险防控与应急技术装备”重点专项“2019-nCoV灭活疫苗”项目的紧急立项 , 随后科研攻关团队加班加点 , 以每天16个小时以上高强度工作的“战时机制”推进疫苗的研发 , 平均每周都能取得一项突破性的进展 。 由于临床前研究的数据较为充分 , 同时也因为全球严峻的疫情防控形势 , 因此国家药监局为中国生物新冠灭活疫苗开通了“绿色通道” , 一次性批准了Ⅰ/Ⅱ期临床试验 。 4月12日 , 中国生物武汉生物制品研究所研发的新冠灭活疫苗成为全球首款进入Ⅰ/Ⅱ期临床试验的疫苗 。 4月27日 , 中国生物北京生物制品研究所研发的新冠灭活疫苗也进入Ⅰ/Ⅱ期临床试验 。 两个疫苗的Ⅰ/Ⅱ期临床研究共入组2240人 。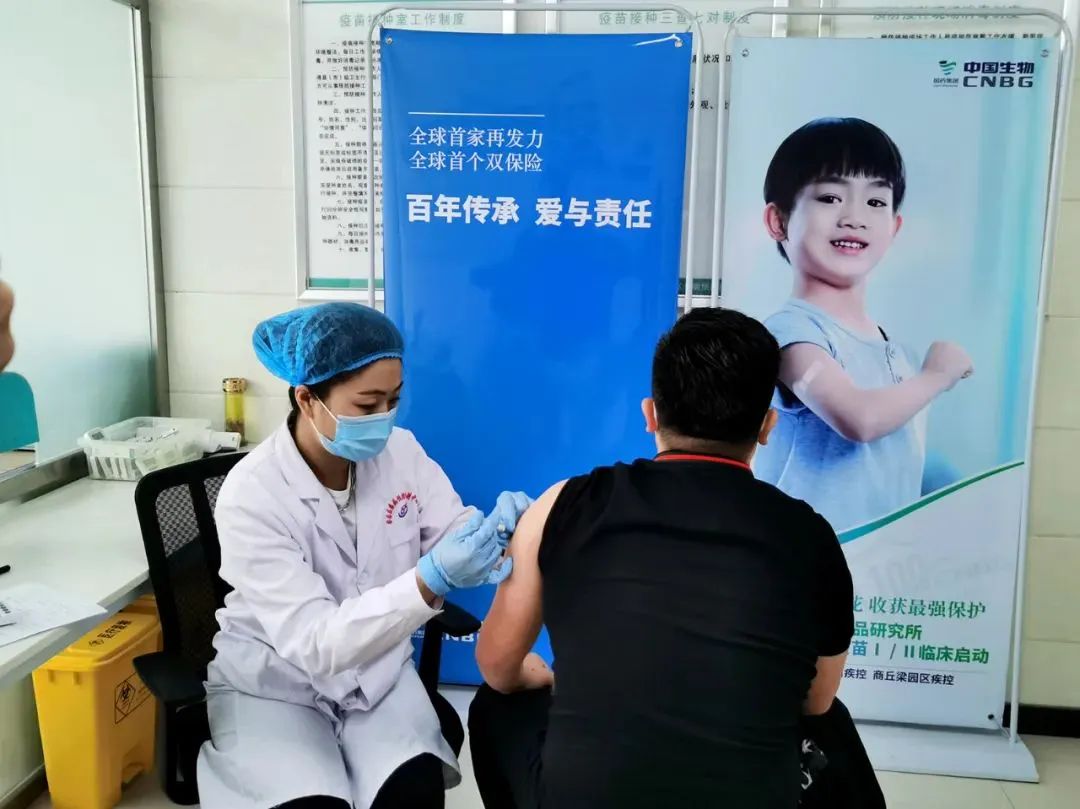
本文图片
6月16日中国生物武汉生物制品研究所Ⅰ/Ⅱ期临床试验阶段性揭盲结果显示:疫苗接种后安全性好 , 无一例严重不良反应 。 不同程序、不同剂量接种后 , 疫苗组接种者均产生高滴度抗体 。 0 , 28天程序接种两剂后 , 中和抗体阳转率达100% 。分页标题
中国生物北京生物制品研究所的Ⅰ/Ⅱ期临床试验结果于6月28日揭盲 。 疫苗接种后安全性好 , 不同程序、不同剂量接种后疫苗组接种者均产生高滴度抗体 , 0 , 21天程序接种两剂后中和抗体阳转率达100% , 0 , 28天程序接种两剂后中和抗体阳转率达100% 。
在Ⅰ/Ⅱ期临床试验逐渐取得可喜成果之后 , 中国生物新冠灭活疫苗研制团队积极推进Ⅲ期临床研究工作 , 开展海外合作 , 与多个新冠肺炎疫情严重国家的有关机构签订了合作框架协议 。 6月23日 , 国药集团中国生物新冠灭活疫苗国际临床(Ⅲ期)阿拉伯联合酋长国启动仪式在中国北京、武汉、阿联酋阿布扎比三地 , 以视频会议方式同步举行 , 阿联酋卫生部长向国药集团中国生物颁发了临床试验批准文件 。 中阿双方现场签署了相关临床合作协议 , 此举也标志着全球首个新冠灭活疫苗国际临床试验(Ⅲ期)正式启动 。
而决定一款疫苗能否大规模推广的核心因素除了疫苗本身的安全性和有效性之外 , 还有疫苗的生产能力 。 在推进疫苗研发的同时 , 国药集团中国生物也在以战时速度推进高等级生物安全生产设施的建设 。
4月15日 , 中国生物北京生物制品研究所仅仅耗时60天建成了全球最大的新冠肺炎灭活疫苗生产车间 , 投入使用后新冠疫苗产能将达到年产1.2亿剂 。 7月1日 , 耗时一百余天 , 全球唯一的新冠疫苗研发实验室和生产车间综合体——中国生物武汉生物制品研究所新冠疫苗研发实验室和生产车间综合体也宣告落成 , 该车间设计产能为年产1亿剂次 。 两座疫苗“兵工厂“的火速建成 , 无疑为我国新冠疫苗的规模化生产 , 满足未来全国乃至全球范围接种需求打下了坚实的基础 。
本文图片
据了解 , 目前中国生物生产的新冠病毒灭活疫苗库存量已达四百余万份 , 这一数字还在不断攀升 , 一旦中国生物新冠病毒灭活疫苗完成三期临床试验获准上市之后 , 可以很快满足国内庞大的接种需求 。
国产新冠病毒灭活疫苗不良反应发生率及程度远低于在研同类疫苗
新冠病毒疫苗尚未上世 , 对于疫苗的种种担忧就已经出现 。 7月3日 , 世卫组织卫生项目紧急负责人迈克尔·瑞安称 , 研究显示29%的新冠病毒样本都出现了D614G变异 。 世卫组织首席科学家苏米娅·斯瓦米纳坦表示 , 实验室研究发现 , 新冠病毒D614G变异可能导致病毒加速复制 , 这意味着可能加强其传播性 。 消息一出 , 引发了许多人关于疫苗尚未上市就已失效的担忧 。
对此 , 杨晓明表示 , 病毒在传播的过程中出现基因组部分位点的变异这是一种常见现象 。 病毒只有在蛋白质水平上发生非常大的变异时 , 相互作用的受体和靶点才可能改变 。 从目前数据来看 , 新冠病毒发生蛋白质水平上大的变异的可能性极低 , 且现在发生的变异都不是关键点的变异 , 所以不足以引起疫苗无效 。 “我们的灭活疫苗能够覆盖目前发现分离到的全部病毒株 , 包括北京新发地疫情发生后分离到的病毒株 。 ”杨晓明称 。
此外 , 杨晓明还表示 , 中国生物在疫苗研发过程中还会进行不同毒株的交叉保护实验 , 也就是用疫苗免疫动物获得的抗血清 , 与不同基因型的毒株做交叉保护实验 , 如果都能够中和 , 那么对疫苗的研发就没有影响 , 如果有的能中和有的不能 , 研究团队将根据研究进展和现实需要 , 及时调整部分疫苗的研发策略 , 从而确保疫苗的有效性 。
而对于公众对国产新冠肺炎灭活疫苗安全性和有效性的关注 , 杨晓明表示 , 为验证新冠肺炎灭活疫苗安全性、有效性 , 助力新冠肺炎灭活疫苗的早日上市 , 此前 , 国药集团所属四级企业党政主要负责人在内的180名志愿者带头接种了新冠灭活疫苗 。 志愿者人体预测试表明 , 受试者抗体已完全达到抵抗新冠病毒水平 。 近期又有1000余名国药集团干部员工自愿接种 , 也都显示疫苗安全有效 , 不良反应发生率及程度远低于在研的同类疫苗 , 这无疑给了研发团队很大的信心 。 此时 , 国产新冠肺炎灭活疫苗还在慎之又慎地推进疫苗的Ⅲ期临床 , 在更大人群范围内验证疫苗的安全性及有效性 , 从目前Ⅱ期临床揭盲结果显示 , 效果是非常好的 。
“中国有一个古老的传说 , 叫神农尝百草 。 中国生物制品工作者就像‘神农尝百草’一样 , 数代中国生物人就是将这种以身试药的献身精神一代一代传承了下来 。 比如说被称为“衣原体之父”的汤飞凡 , 正是凭着这种以身试药、以身试毒的精神 , 将沙眼病毒种到自己眼中的 , 而成为世界上发现重要病原体的第一个中国人 。 基因工程重组宫颈癌疫苗试制出来后 , 中国生物全课题组的十几个年轻人不分男女 , 每个人都先给自己来一针 。 这种以身试药一方面是为医药事业献身的精神 , 另一方面也是我们对研发的疫苗有信心 , 我觉得这是献身精神和科学精神的结合 。 ”杨晓明称 。
新冠病毒灭活疫苗研发 , 不是在以年、月计 , 而是在以小时计
通常而言 , 一款新疫苗从立项、研发到试验评估、行政审批 , 直到上市 , 全过程需要8~10年时间 。 而中国生物的新冠病毒灭活疫苗 , 从立项到获批临床试验 , 仅仅只用了98天 , 在尊重研发规律完成至少六个月的三期临床试验之后 , 中国生物有望用一年左右的时间完成一款疫苗的研发流程 , 这种研发速度堪称奇迹 。分页标题
在谈到中国生物为何能够如此高效地完成新冠病毒疫苗研发工作时 , 杨晓明表示 , 这一次的疫苗攻关战 , 淋漓尽致地展现了我们国家集中力量办大事、举国体制的巨大优势 。
在疫苗的攻关阶段中 , 各研发单位、合作单位、生产单位以及科技主管部门、医卫监管部门等各方均全盘通力配合、全力以赴 , 通过集中力量、串联转并联的方式 , 加速疫苗研发 。 比如在疫苗的有效性评价环节 , 以往的方式是对不同种类的动物逐一进行有效性试验 , 这次采用并联的方式后 , 则是对不同种类的动物同时开展有效性试验 。
再比如疫苗制备完成后 , 以往是研发机构要先自己检定合格 , 再送到中国食品药品检定研究院进行检定 , 这一次是研发机构在自己检定的同时 , 送到中检院同步进行检定 , 从而缩短了检验周期 。
“国家药监局在晚上7点钟给我们颁发了可以进入Ⅰ/Ⅱ期临床试验的批件 , 当晚9点我们就给志愿者接种了第一针 。 疫苗在获得临床试验批件之前 , 地方疾控部门就把参与试验的志愿者全部动员到位 , 可以说 , 各单位都是不讲任何条件 , 积极主动地履行职责 , 各环节之间的工作实现了高效、无缝的衔接 。 ”杨晓明称 。
其次 , 这一次新冠病毒疫苗研发进展如此之快 , 也有赖于我们多年持续不断的大规模科研投入 , 建立了多个成熟的技术平台和人才团队 , 疫苗研发的整条产业链都取得了长足进步 。 工艺、质量监督体系也在不断更新 , 均保持全球先进水平 。 这一次新冠病毒疫苗攻关战中 , 我国采用灭活疫苗、重组蛋白疫苗、腺病毒载体疫苗、减毒流感病毒载体活疫苗、核酸疫苗5条技术路线并举的方式推进疫苗开发 。 仅中国生物一家就同时在四条技术路线上马不停蹄的攻关 , 展示出深厚的科研实力 。
“如果说疫苗研发是‘一边开飞机、一边造飞机’ , 那么研发环节相关的‘零件’等供应链都要及时跟上 。 近年来 , 疫苗相关产业链配套逐渐齐全起来 。 回想30多年前 , 我在兰州生物制品研究所研发疫苗 , 试验室里几乎所有要用到的仪器、设备、试剂都要从国外进口 , 中间耗时长达数月 , 想快都快不起来 。 “杨晓明称 。
我们不是在和美国赛跑 , 而是在和病毒赛跑
在新冠病毒疫苗成为终结疫情“救命稻草”已成共识的背景下 , 全球少数几个具备研发新冠病毒疫苗科研实力和经济基础的国家无形之中就被赋予了各种“期望” 。 当下 , 中美两国各自因为有多款疫苗率先进入三期临床试验而被公众视为最有可能 “扮演”拯救世界角色的国家 , 中美之间的疫苗研发进度之争自然而然就成为外媒炒作的热点 。
5月4日 , 美国“商业内幕”网站刊文将中美两国的疫苗研发工程称为是一场类似于“登月竞赛”那样的国力之争 , 文章还援引一位全球公共领域卫生专家的话称 , 谁能在疫苗研发上“夺魁” , 就将在地缘政治上获得巨大优势 , 美国安全官员和顶尖的医疗卫生专家都在担心 , 若中国首先获得成功 , 将使美国处于极为不利的地位 。
对于外媒热衷炒作的中美疫苗之争的话题 , 杨晓明表示 , 中国很早就向世界庄严宣告 , 中国新冠疫苗研发完成 , 并投入使用后 , 将作为全球公共产品 , 为实现疫苗在发展中国家的可及性和可担负性作出中国贡献 。 中国在疫苗研发上 , 也采取的是与有需求的国家携手同行的路线 , 大家共同寻找应对新冠肺炎大流行的关键解决方案 。
而作为新冠病毒疫苗研发的一位“种子选手” , 中国生物本身也拥有多个国际认证的疫苗产品品种 , 与许多国际机构疫苗项目有过成功的合作案例 , 具有大规模向国外出口疫苗的经验 。 当下 , 中国生物已在北京、武汉两地建设完成新冠灭活疫苗生产车间 , 年产能达2亿剂 。 一旦疫苗成功上市 , 很快就能够大批量地为全世界提供安全、有效、高质量的疫苗 , 并不会奇货可居 , 不会在世界各国饱受新冠肺炎疫情折磨的时候利用自身的技术优势去谋求某种利益 。
“所以 , 我并不认为新冠病毒疫苗的快速研发有中美之争 , 我们不是在和美国赛跑 , 而是在和病毒赛跑 。 ”杨晓明称 。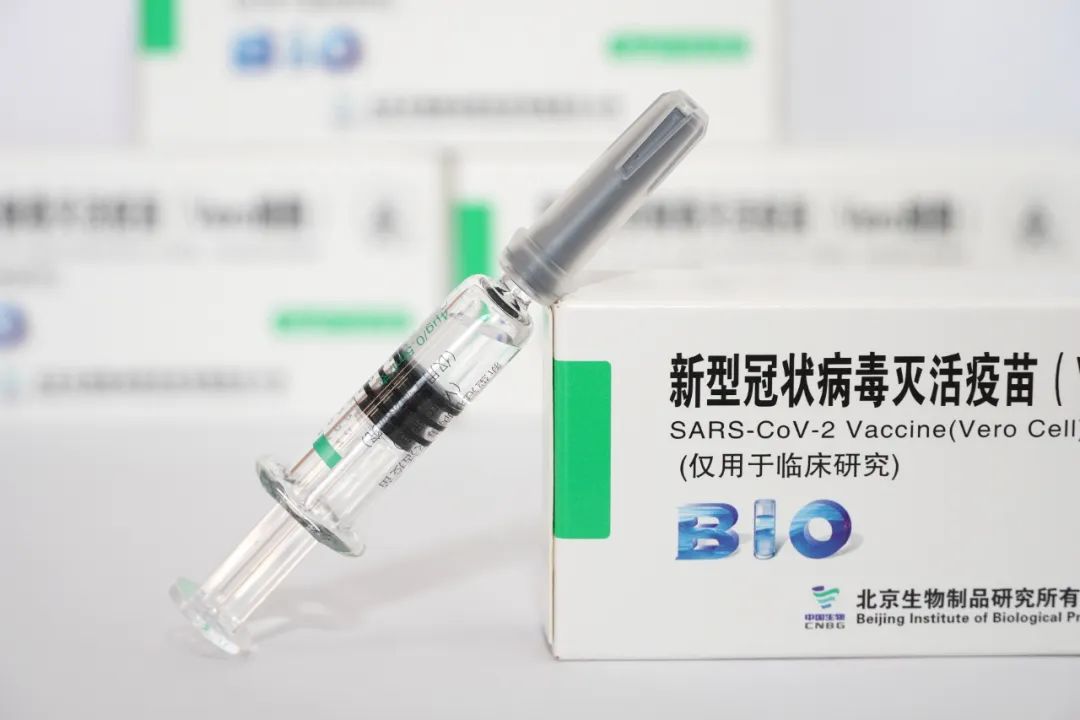
本文图片
【临床实验|媒体披露国产疫苗最新消息:进度全球领先,具备大规模量产能力】
