按关键词阅读:
在乙肝一线药物研发至今 , 核苷酸类似物(NAs)占据80%的乙肝治疗药物市场 , 还有一种以干扰素为代表可获得更高的e抗原、表面抗原血清转化率药物 , 因其适应症较NA窄 , 副作用以及给药方式不便等原因 , 导致其兼具免疫调节机制的优势没有被真实发挥在乙肝一线药物中 。
文章图片
乙肝干扰素作用潜在机制 , 简介研发历程 , 具有抗病毒作用
干扰素的发现 , 对人类是具有相当意义的 。 早在1957年 , 英国生物学家和瑞士研究人员 , 使用鸡胚绒毛尿囊膜研究流感干扰治疗时发现 , 流感病毒感染的细胞可以产生一种因子并作用于其他细胞 , 能够感染流感病毒复制 , 因而将其命名为干扰素 。 直到1966年至1971年间 , 另一位科学家Friedman阐述了干扰素的抗病毒机制 , 并引发药物学界对其更广泛使用的关注 。
药物学家发现 , 干扰素兼具免疫调节及抗病毒、抗肿瘤作用 , 在1976年首次报道了人类使用人白细胞干扰素治疗4名慢性活动性乙肝患者 , 研究结果为干扰素治疗后有2名e抗原清除 。 当然 , 医药学界发现干扰素的原料来源较为受限 , 导致其价格高昂 , 随后并未广泛使用于临床治疗 。 但是 , 自1987年开始 , 人类使用基因工程法生产干扰素并进入工业用途 , 这也是首次将干扰素广泛进入市场 。
文章图片
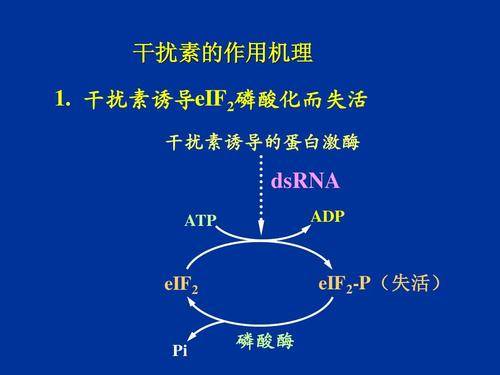
干扰素 , 英文简称IFN , 医学家发现IFN在针对免疫功能低下的慢性乙肝患者身上使用后 , 除观察到抗病毒作用外 , 还观察到其可增加肝细胞膜上白细胞组织相容性抗原密度 , 促进免疫T细胞溶解感染性肝细胞 。 2005年 , 美国FDA正式批准聚乙二醇干扰素α-2a用于治疗成人慢性乙肝领域药物 。 小番健康认为 , 作为一名科研工作者 , 发现干扰素及其研究、应用过程对各种疾病治疗是具有里程碑意义的 。
2020年7月 , Wenyu Wu、Di Wu、Weiming Yan、Yongli Wang等10位研究人员在线发表了关于miR-574外显体将干扰素介导的抗HBV活性从巨噬细胞转移到HBV感染的肝细胞 , 这项研究成果已经在《传染病杂志》( The Journal of Infectious Diseases,简称JID) 。 本研究人员认为 , 干扰素-α(IFN-α)是具有抑制乙肝表面抗原(HBsAg)、HBV-共价闭合环状DNA(cccDNA)作用的 。
文章图片
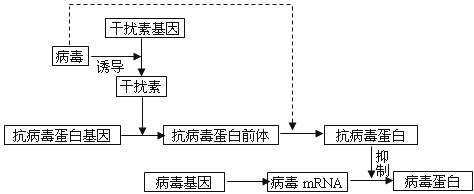
干扰素-α已经被医药学界证明是治疗慢性乙肝(CHB)患者的有效药物 。 然而 , 干扰素-α的潜在作用机制比较模糊 , 这项科研成果也是为了证实其有效性和抗病毒活性 。 研究人员通过观察有反应者和无应答者 , 外显体对聚乙二醇化干扰素α(PegIFN-α)、人白血病单核细胞株THP-1(人白血病单核细胞系)来源巨噬细胞上清液的抗病毒活性 。
然而使用miRNA测序分析了外体microRNAs(miRNAs)的表达谱 。 并使用荧光素酶报告法 , 定位被鉴定的miRNA靶向的乙肝病毒基因组序列的结合位置 。 研究结果表明 , PegIFN-α在治疗所有患者的外显子体时 , 尤其是应答者 , 以及IFN-α处理的巨噬细胞上清具有抗病毒活性 , 表现为抑制乙肝病毒相关细胞系中的乙肝表面抗原、e抗原、HBV-DNA和cccDNA水平 。
PegIFN-α治疗 , 上调了外显体hsa-miR-193a-5p、hsa-miR-25-5p和hsa-miR-574-5p , 它们可以部分抑制乙肝病毒复制和转录 。 此外 , Hsa-miR-574-5p通过与乙肝病毒基因组序列中的2750-2757位点结合 , 进而降低pgRNA和聚合酶mRNA的水平 。 因此 , 本研究最终结论是 , 外显子能将IFN-α相关miRNA从巨噬细胞转移到乙肝病毒感染的肝细胞中 , 具有抗病毒作用 。 
稿源:(小番健康)
【】网址:http://www.shadafang.com/c/hn110E9AN2020.html
标题:作用|乙肝干扰素作用潜在机制,简介研发历程,具有抗病毒作用
