在新冠病毒出现近2年以后,我们终于有了能对抗它的“特效药”。
11月4日,美国默克公司宣布,其与合作伙伴里奇巴克生物医药公司(Ridgeback)共同研发的口服抗新冠病毒药物莫那比拉韦(Molnupiravir)获得英国药监局批准上市,成为全球第一款获批用于治疗成人轻度至中度新冠感染的口服药物。
紧接着,11月5日,美国辉瑞公司宣布,其研发的新冠口服抗病毒候选药物Paxlovid,可以使新冠高危患者的住院、死亡风险降低89%。
而今,我国的新冠特效药也有望在12月底前获得批准附条件上市。据媒体报道,由清华大学、深圳市第三人民医院和腾盛博药合作研发的新冠药物BRII-196和BRII-198联合用药临床Ⅲ期已揭盲,给药组在治疗28天后实现零死亡,对照组8例死亡,详细结果会在近期对外公布。
大多特效药为“老药新用”
美国默克公司研发的Molnupiravir是一种针对RNA病毒的小分子广谱抗病毒口服药,可抑制新冠病毒的复制。
中国南方医科大学副校长、广东省药理学会理事长刘叔文介绍,新冠病毒是一种RNA(核糖核酸)病毒,Molnupiravir可在新冠病毒基因组中“掺假”,并诱导其产生错误突变以破坏基因组复制,从而抑制病毒传播。
根据默克公司10月1日公布的Ⅲ期临床试验中期分析数据,该药可将轻中症新冠患者住院/死亡风险降低约50%,对变异新冠病毒德尔塔、伽马和缪毒株也显示出一致的疗效。
美国辉瑞公司研发的Paxlovid由小分子药物PF-07321332和利托那韦组成,前者是针对新冠病毒主蛋白酶的抑制剂,利托那韦则是抗病毒药增效剂,此前曾用于抗艾滋病病毒。
与Molnupiravir相比,Paxlovid的疗效更优:Ⅱ/Ⅲ期临床试验中期分析结果显示,口服Paxlovid能降低89%的住院和死亡风险。
文章插图
(图源:辉瑞官网)
但不管是默克公司的Molnupiravir,还是辉瑞公司的Paxlovid,其实都是“老药新用”的结果。
Molnupiravir的研发可追溯到2014年,是在筛选抗委内瑞拉马脑炎病毒药物时发现的;Paxlovid则是此前针对SARS 病毒研制的蛋白酶抑制剂,在此基础上开发出新冠病毒转录抑制剂。
除此以外,英国《柳叶刀·全球健康》10月27日刊载一份来自巴西的研究报告称,常用抗抑郁药氟伏沙明(fluvoxamine)可显著降低新冠患者的重症/死亡风险。新冠早期患者服药后病死风险可降低约90%,重症住院风险可降低约65%。
文章插图
(图源:柳叶刀)
英国《自然》杂志报道称,氟伏沙明可抑制免疫反应和缓解组织损伤,而免疫系统过度反应导致的炎症因子风暴是造成新冠重症和死亡的重要因素。
之所以这么多的“老药新用”,是因为抗病毒特效药的研发周期一般特别长,从搞明白新冠病毒感染人体细胞的途径,到漫长的动物实验及三期临床实验,这个周期至少有10年之久,而若是从“老药”入手,时间进程就会大大缩短。
国产“特效药”的研发进程
据央视财经报道,目前我国自主研发的新冠特效药已有六种,而其中已有四种进入Ⅲ期临床试验阶段,分别为开拓药业的普克鲁胺、真实生物的阿兹夫定、腾盛博药的BRII-196/BRII-198、神州细胞的SCTA01。
在这其中,目前进展最快的是清华大学、深圳市第三人民医院和腾盛博药联合研发的BRII-196/BRII-198,这是一种中和抗体联合疗法,可有效阻碍新冠病毒进入人体细胞。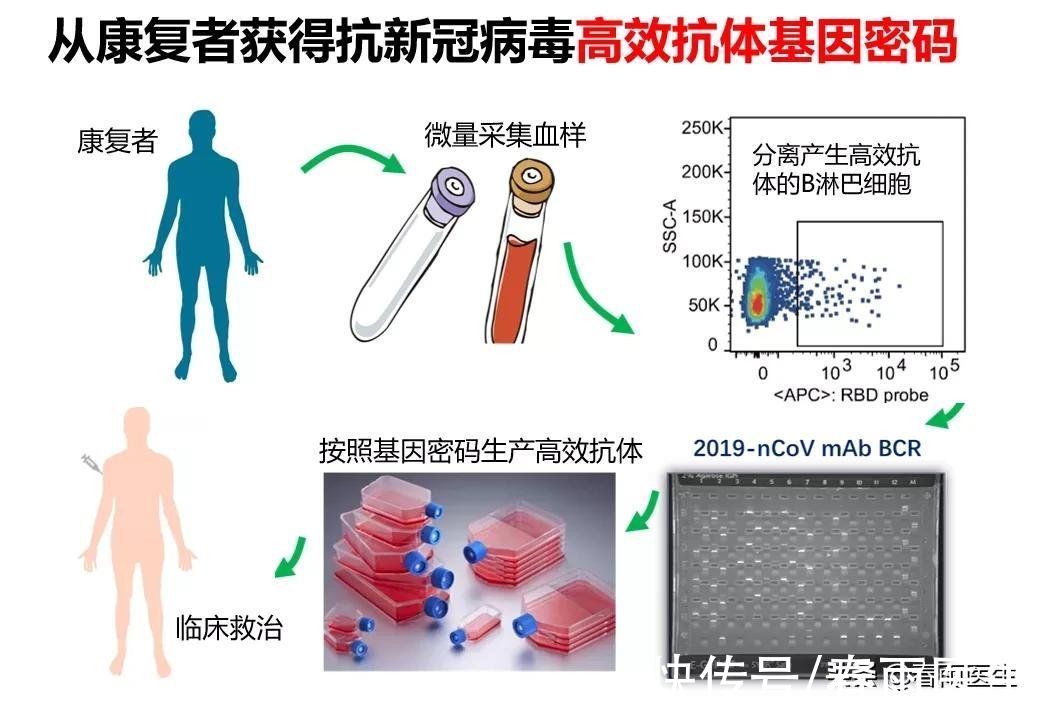
文章插图
(团队研制新冠特效药候选药流程示意图/图源:科技日报)
据报道,由美国国立卫生研究院(NIH)主导该药的Ⅲ期临床试验正在美国、巴西、菲律宾等7个国家展开,研究结果乐观,BRII-196和BRII-198的联合治疗可降低78%的住院和死亡率,最有可能率先在美国等发达国家获得紧急使用授权。
而在国内,研发团队也已于10月9日向国家药监局滚动提交附条件上市申报材料,有望12月底前获得批准(附条件)上市。
此外,开拓药业的普克鲁胺是用于治疗新冠肺炎重症患者的小分子口服药物。现有临床试验数据显示,普克鲁胺可在体内减轻免疫炎症反应和组织损伤,提示其对于重症新冠肺炎具有可能的治疗机制。普克鲁胺有望成为轻、中、重症新冠肺炎患者全疾病周期的治疗药物。
阿兹夫定是一种艾滋病病毒逆转录酶抑制剂,2020年4月中旬,国家药监局批准阿兹夫定的Ⅲ期临床试验,用于治疗新冠肺炎。2020年10月,《Nature》子刊发表的研究论文详细介绍了阿兹夫定治疗新冠肺炎的研究进展,称阿兹夫定可实现新确诊患者快速核酸转阴。
- 推荐|2021年以来,推荐展示活动联动多家连锁药店……
- 新冠病毒|警惕!刚刚通报:又一地出现奥密克戎
- 女人越来越“花心”的原因,看完你就知道了
- 三河市|河北省三河市新增3例新冠肺炎确诊病例,行动轨迹公布
- 世卫:疫情三月将结束,建议取消国际旅行限制!话音刚落,“奥密克戎的妹妹”来了……
- 《我的前半生》:全职太太的经济来源是什么?
- 为什么有些女人婚后变得越来越孤独?
- 被背叛的痛,到底能够带来怎样的成长?
- 河北区|天津河北区新增1例新冠肺炎确诊病例
- 三河市|河北三河市新增3例新冠肺炎确诊病例 行程轨迹公布
