里程碑突破!中国专家造出了抗癌药,实现长期生存,在美率先上市
泽布替尼中国自主研发的新一代BTK抑制剂 , 适用于慢性淋巴细胞白血病(CLL)及套细胞淋巴瘤(MCL)的治疗 。
上个月 , 权威杂志《血液(Blood)》连续发表2篇文章 , 公布了泽布替尼治疗华氏巨球蛋白血症(WM)的3年随访数据 , 证实其优异的疗效以及安全性 。
 文章插图
文章插图
一、抗癌效果好 , 美国率先上市在此之前 , 泽布替尼的临床试验是在我国及欧美国家同步进行的 , 随着欧美临床试验的先期完成 , 2019年 , 泽布替尼率先获得美国FDA的批准而上市 。 2020年6月 , 泽布替尼在国内正式批准上市 。
 文章插图
文章插图
在针对华氏巨球蛋白血症的临床试验中 , 一共纳入了77名晚期患者 , 根据治疗的标准 , 每个患者每天服用两次药物 , 每次的剂量是160mg 。 截至到今年11月底 , 还有72.7%的患者仍旧在接受治疗 , 其余终止治疗的患者中 , 不良反应的占13% , 疾病进展的占10.4% , 其他原因的占3.9% 。
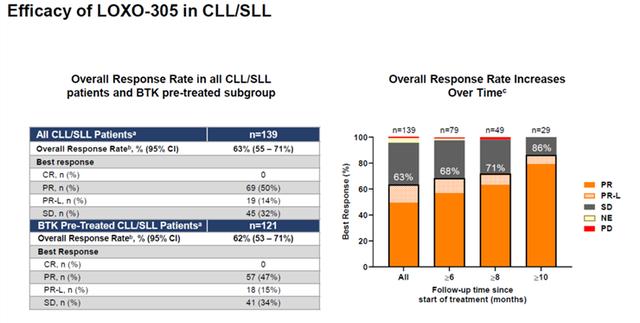
最终的试验结果表明 , 泽布替尼的客观缓解率达到95.9% , 完全缓解率是45.2% , 并且随着用药延长还会持续增长 , 这说明泽布替尼的持久和良好疗效 , 安全性良好 。
 文章插图
文章插图
而早前在针对B细胞淋巴瘤的试验中 , 泽布替尼的完全缓解率达到了59% , 总缓解率是84% , 而且相比其他药物 , 不良反应的发生率更低 , 已有部分患者基本实现了临床治愈和长期生存 。
二、60年前的意外发现 , 中国团队成功开发泽布替尼的问世 , 和60年前的一次意外发现有着千丝万缕的联系 。
1952年 , 一名患有严重败血症并且反复感染的8岁男孩 , 被送到了儿科医生欧格登·布鲁顿(Ogden Bruton)这里 。 布鲁顿认为 , 患者的免疫力有着某种先天性的缺陷 , 后来的分析表明 , 患者体内缺乏丙种免疫球蛋白 , 这是人类首次对这种疾病的记录和诊断 。
 文章插图
文章插图
图:Ogden Bruton医生
虽然当时利用注射免疫球蛋白的方式 , 可以对患者进行治疗 , 但由于医疗技术限制 , 没人知道是什么原因导致了这种疾病的发生 。
1953年 , 随着DNA双螺旋结构的揭示 , 科研人员分离出了导致这种免疫缺陷的基因 , 它本身的编码是一类酪氨酸激酶 。 为了纪念这种疾病的最初记录者 , 所以将这种酶类命名为“布鲁顿氏酪氨酸激酶” , 缩写是BTK 。
随着研究深入 , 科学家发现 , BTK是B细胞受体信号通路的关键组成部分 , 一旦BTK失去作用 , 细胞会出现异常 , 而一旦BTK过度活跃 , 同样会导致病变 。
 文章插图
文章插图
在白血病、淋巴瘤患者的癌细胞中 , 相关细胞通路就异常活跃 , 而BTK发挥了推波助澜的作用 。 此后 , 在慢性淋巴细胞白血病的患者体内 , 同样发现了类似的特性 。 于是 , BTK就成为了开发抑制剂治疗癌症的新靶点 。
在研发的初始阶段 , 泽布替尼选择的靶点就是BTK , 因为这是一个明确的靶点 , 在此前的试验中得到了验证 。
2012年7月 , 该研发项目正式开启 。 5个月后 , 一款新的分子命名为BGB-3111诞生了;
2014年 , 第一批临床试验在澳大利亚开展;
2016年 , BGB-3111有了正式名字 , 泽布替尼;
2017年 , 全球三期临床试验启动;
2019年 , 泽布替尼在美国正式获批上市 。
2020年 , 泽布替尼在国内正式获批上市 。
- 也门:一个几乎全民嚼食毒品的国家
- 中国每天有1万人确诊癌症,医生忠告,想长寿,睡前请坚持五不要
- 中国胸壁外科联盟陕西地区联盟成立仪式在西安市红会医院顺利召开
- 家中常备“维C”补品,如何正确打开,没几个人说得上来
- 好莱坞那些看不起中国,新片上映后却为了钱来华宣传的双面人明星
- 肝癌有新突破!我国揭示肝癌复发与3种细胞有关,成治疗新依据
- 中国总计约有4亿肝病患者!医生提示:早晚两不要,肝脏才会更好
- 重庆日报党委委员、编委雷太勇:坚守媒体责任担当,助力健康中国事业
- 围绕中国肝癌诊疗领域最高级别指导文件,顶尖专家今聚上海,强调肝癌规范诊治
- 乙肝病毒百万携带者,2个月转阴,中医治疗乙肝再获突破
